Il termine collagene (o collageno) indica una famiglia eterogenea di glicoproteine della matrice extracellulare (ECM). In tutte le sue forme, il collagene è la proteina più abbondante negli animali, costituendo circa il 25-30% della massa proteica totale (nell’essere umano corrisponde a circa il 6% del peso corporeo complessivo). Nel corpo dei vertebrati è il principale costituente di pelle, tendini, cartilagini e ossa [Exposito].
Il collagene è insolubile in acqua ed è anche resistente in vitro all’azione degli enzimi digestivi. Il trattamento termico e/o l’azione di acidi, alcali o specifici enzimi causano una parziale degradazione del collagene con rottura di alcuni legami covalenti, portando alla formazione di gelatina, una miscela eterogenea di peptidi più solubile del materiale di partenza. La gelatina è spesso utilizzata in alimenti, prodotti farmaceutici, pellicole fotografiche e cosmetici. Un’ulteriore e più estesa degradazione enzimatica della gelatina produce il collagene idrolizzato (o gelatina idrolizzata o ancora peptidi di collagene) [Shigemura4].
Il termine collagene deriva dal greco κόλλα, che significa “colla”, e dal suffisso -γέν, che significa “produrre”. Infatti, già 3000 anni fa, gli Egizi utilizzavano soluzioni di gelatina come colla per riparare oggetti in legno [Silvestrini].
La gelatina è utilizzata come alimento da moltissimo tempo. L’aspic, prodotto bollendo teste di pesce, fu introdotto come piatto di alta classe in un libro di cucina di Baghdad datato intorno al X secolo. L’uso moderno della gelatina per i dessert risale al XVIII secolo, periodo nel quale divenne possibile la produzione di massa di gelatina [Kubo].
La struttura del collagene
Formato da 19 dei 20 amminoacidi proteinogenici (con l’eccezione del triptofano1) e da quantità significative di alcuni aminoacidi inusuali, tra cui idrossiprolina (Hyp) e idrossilisina (Hyl), il collagene ha una struttura molto robusta che conferisce elasticità, tonicità e resistenza a tutti i tessuti umani. Gli aminoacidi presenti in maggior quantità nel collagene sono la glicina (Gly) e la prolina (Pro).
Finora sono stati identificati 29 tipi di collagene [Shenoy] (v. tab. 1).
Sulla base delle loro conformazioni, i tipi di collagene attualmente identificati vengono generalmente classificati in uno dei seguenti tre gruppi: collagene fibroso (o fibrillare), collagene associato alle fibrille e collagene della membrana basale.
I collageni fibrillari (chiamati così perché sono organizzati in fibrille) e il collagene (non fibrillare) di tipo IV (caratteristico della membrana basale della ECM) sono stati descritti in tutti gli animali dalle spugne fino agli esseri umani [Exposito, Sutmuller].
I collageni fibrillari, come i tipi I e III, svolgono un ruolo fondamentale nella meccanica strutturale dei tessuti umani. Il collagene di tipo I è il più abbondante nel corpo umano; i tipi I e III, entrambi fibrillari, costituiscono oltre il 90% del collagene umano [Wikipedia].
|
Tipo |
Note |
|
I |
Questo è il tipo di collagene più abbondante del corpo umano. È presente nei tendini, nella pelle, nelle pareti arteriose, nella cornea, nell’endomisio che circonda le fibre muscolari, nella fibrocartilagine e nella parte organica di ossa e denti; è il prodotto finale dei processi di riparazione dei tessuti ed è presente nel tessuto cicatriziale. |
|
II |
Cartilagine ialina, costituisce il 50% di tutte le proteine della cartilagine. Umor vitreo dell’occhio. |
|
III |
Questo è il collagene del tessuto di granulazione e viene prodotto rapidamente dai fibroblasti giovani prima che venga sintetizzato il collagene di tipo I più resistente. Fibra reticolare. Si trova anche nelle pareti arteriose, nella pelle, nell’intestino e nell’utero. |
|
IV |
Lamina basale; cristallino. Svolge anche in parte la funzione di filtrazione nei capillari e nei glomeruli del nefrone del rene. |
|
V |
La maggior parte del tessuto interstiziale, associato al tipo I, associato alla placenta. |
|
VI |
La maggior parte del tessuto interstiziale, associato al tipo I. |
|
VII |
Forma le fibrille di ancoraggio nelle giunzioni dermoepidermiche. |
|
VIII |
Alcune cellule endoteliali. |
|
IX |
Collagene FACIT, cartilagine, associato con fibrille di tipo II e XI. |
|
X |
Cartilagine ipertrofica e in fase di mineralizzazione. |
|
XI |
Cartilagine. |
|
XII |
Collagene FACIT, interagisce con le fibrille contenenti collagene di tipo I, decorina e glicosaminoglicani |
|
XIII |
Collagene transmembrana, interagisce con l’integrina a1b1, la fibronectina e i componenti delle membrane basali come il nidogeno e il perlecano. |
|
XIV |
Collagene FACIT, noto anche come undulina |
|
XV |
– |
|
XVI |
Collagene FACIT. |
|
XVII |
Collagene transmembrana, noto anche come BP180, una proteina da 180 kDa. |
|
XVIII |
Fonte di endostatina. |
|
XIX |
Collagene FACIT. |
|
XX |
– |
|
XXI |
Collagene FACIT. |
|
XXII |
Collagene FACIT. |
|
XXIII |
Collagene MACIT. |
|
XXIV |
– |
|
XXV |
– |
|
XXVI |
– |
|
XXVII |
– |
|
XXVIII |
– |
|
XXIX |
Collagene epidermico. |
Tabella 1: Tipi di collagene conosciuti e tessuti correlati (adattato da [Shoulders, Wikipedia])
Dal punto di vista strutturale, tutti i tipi di collagene sono formati da unità proteiche costituite da tre catene polipeptidiche (catene α), identiche o meno tra loro, che si intrecciano a formare una struttura che contiene almeno un dominio a tripla elica [Exposito].
Le parti di catena α coinvolte nella formazione della struttura a tripla elica sono costituite da sequenze di triplette Gly-X-Y (dove Gly è una glicina e X e Y sono due generici aminoacidi) formanti il cosiddetto dominio collagenoso [Exposito]. Le posizioni X e Y sono per lo più occupate rispettivamente dalla prolina (Pro) e dall’idrossiprolina (Hyp) [Taga].
Nei collageni fibrillari le catene α sono tipicamente costituite da una porzione centrale collagenosa composta da una sequenza ininterrotta di triplette Gly-X-Y che si avvolge su se stessa a formare una elica sinistrorsa, affiancata da due domini non collagenosi (non costituiti, cioè, da sequenze Gly-X-Y). Le catene si assemblano poi in gruppi di tre avvolgendosi insieme a formare strutture costituite da un unico dominio a tripla elica destrorsa affiancato da due porzioni non spiralizzate (telopeptidi). Tali strutture costituiscono il tropocollagene2 [Exposito, Quan].
Biosintesi del collagene
Il collagene viene sintetizzato da diversi tipi di cellule a seconda del tessuto (ad esempio, i fibroblasti nel tessuto connettivo, gli osteoblasti nell’osso). In particolare, la biosintesi del collagene avviene in più fasi, alcune delle quali intracellulari e altre extracellulari.
Per i tipi di collagene fibrillare, il processo è schematicamente il seguente.
- Dapprima vengono prodotte le catene α (indicate come α1, α2 o α3) che vengono sintetizzate dai ribosomi situati sulla superficie esterna del Reticolo Endoplasmatico Ruvido (RER) come pre-pro-peptidi con forma di filamenti tridimensionali (procatene o preprocollagene). I pre-pro-peptidi vengono successivamente rilasciati nel lume del RER, dove vengono trasformati in propeptidi mediante la scissione della sequenza segnale N-terminale (la prima parte del filamento proteico) [Carlson].
- All’interno del RER, i propeptidi sono sottoposti, durante il loro allungamento, ad alcune modificazioni post-traduzionali: alcune lisine e alcune proline dei propeptidi vengono idrossilate rispettivamente dagli enzimi lisil idrossilasi e prolil idrossilasi, producendo idrossilisina (Hyl) e idrossiprolina (Hyp3). Entrambi questi enzimi richiedono la vitamina C come cofattore4. Questo passaggio contribuisce alla reticolazione delle catene α e alla stabilizzazione della tripla elica, ed è il motivo per cui il collagene contiene quantità significative degli amminoacidi inusuali Hyp e Hyl. Mentre l’idrossilazione delle proline in posizione Y è la norma, quella in posizione X è molto meno comune, tant’è vero che è presente un solo residuo di questo tipo per catena nei collageni I e II, a differenza del collagene IV che ne presenta diversi [Carlson, Harwood, Hulmes, Michelacci].
- La frequenza della modifica post-traduzionale dei residui prolilici e lisilici varia in maniera importante tra i diversi tipi di collagene. Ad esempio, la frequenza dell’idrossilazione dei residui di lisina nel collagene di tipo IV è molto elevata (oltre il 90% dei residui in posizione Y è idrossilato), mentre nei tipi I e III solo il 15% è idrossilato [Michelacci].
- I residui di lisina idrossilata (ma non di Hyp) possono essere successivamente ulteriormente modificati da specifici enzimi (galattosil transferasi e galattosilidrossilisil-glucosil transferasi5) del reticolo endoplasmatico che aggiungono galattosio e glucosio al gruppo ossidrile dei residui di idrossilisina, per formare galattosilidrossilisina e successivamente glucosilgalattosilidrossilisina (quindi, entrambi O-glicosidi) [Canty, Carlson, Harwood].
- Inoltre, nelle estensioni propeptidiche possono essere presenti anche altri oligosaccaridi. Questi oligosaccaridi vengono sintetizzati su un intermedio dolicolico nella membrana del RER e trasferiti intatti alla catena pro-α. Si ha una scissione iniziale dell’oligosaccaride mentre la catena si trova ancora nel RER e una ulteriore successiva elaborazione nell’apparato del Golgi [Michelacci].
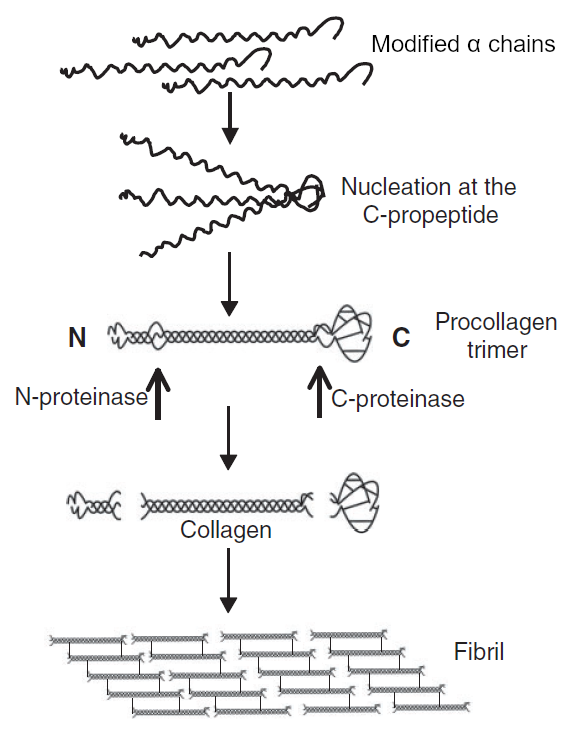
Fig. 1: Biosintesi del collagene, step 6-11 (adattato da [Canty])
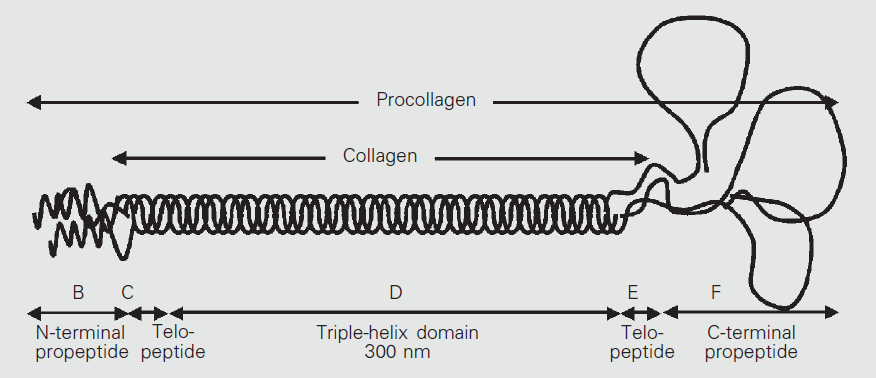
Fig. 2: Procollagene di tipo I (adattato da [Michelacci]) - Successivamente, tre delle catene α modificate si avvolgono insieme formando il procollagene (figg. 1,2). La neo-formata struttura del procollagene è costituita da un’elica centrale destrorsa (dominio a tripla elica), lunga circa 300 nm, composta esclusivamente dalle sequenze (Gly-X-Y)n della catena α, affiancata da due sequenze terminali globulari non spiralizzate, che non presentano il motivo ripetuto Gly-X-Y, una a ciascuna estremità della catena (propeptidi N e C) [Canty, Carlson, Hulmes].
- La formazione di legami disolfuro tra i peptidi C-terminali delle catene α porta i tre peptidi in una disposizione favorevole alla formazione dell’elica (nucleazione). L’avvolgimento della tripla elica del collagene è direzionale e avviene nella direzione C-N (fig. 1). Le tre catene α possono essere identiche tra loro (collagene omotrimerico, come nel collagene III che è composto da tre catene α1(III)) o differenti (collagene eterotrimerico o eterotipico, come nel collagene I che è composto da due catene α1(I) e una catena α2(I))6 [Canty, Carlson].
- Le molecole di procollagene vengono traslocate nell’apparato di Golgi, dove gli oligosaccaridi aggiunti durante la fase 5 vengono tagliati e si procede alla sintesi di una struttura ad alto contenuto di mannosio. Inoltre, in alcuni tipi di collagene alcuni residui di serina vengono fosforilati e alcuni di tirosina vengono solfatati. Successivamente, il procollagene viene impacchettato in vescicole secretorie che, fondendosi con la membrana cellulare, rilasciano il loro contenuto nell’ambiente extracellulare (esocitosi) [Carlson, Michelacci].
- Al di fuori della cellula, alcuni enzimi di membrana (proteinasi del procollagene N e del procollagene C) rimuovono la maggior parte delle estremità globulari del procollagene, lasciando solo due piccoli residui (telopeptidi) della porzione non avvolta presente a ciascuna estremità, producendo il tropocollagene, una molecola che quindi consiste in un singolo dominio a tripla elica affiancato da due corte porzioni terminali telopeptidiche: telopeptide N (situato all’estremità N-terminale) e telopeptide C (situato all’estremità C-terminale del procollagene). I telopeptidi costituiscono circa il 2-5% della molecola di tropocollagene ed influenzano l’assemblaggio e la stabilità delle fibrille (figg. 1,2) [Canty, Carlson].
- Successivamente, le molecole di tropocollagene si aggregano rapidamente in strutture ordinate, disponendosi una dopo l’altra, orientandosi grazie alla presenza dei telopeptidi (il telopeptide N si oppone al telopeptide C) e disponendosi in file parallele, formando strutture simili a stringhe chiamate fibrille (fig. 1).
- All’interno delle fibrille, l’impacchettamento del tropocollagene è caratteristicamente sfalsato di una distanza regolare, pari a 1/4 della lunghezza molecolare, rispetto alle molecole adiacenti (fig. 1). L’impacchettamento con sfalsamento di un quarto e l’intero processo di formazione delle fibrille sono processi non enzimatici e sono guidati e stabilizzati da un gran numero di legami non covalenti su tutti i lati delle molecole a bastoncino impacchettate all’interno di ciascuna fibrilla, anche se la natura delle interazioni che regolano il diametro delle fibrille non è completamente stata completamente chiarita [Carlson, Michelacci].
- Le molecole di collagene disposte secondo la matrice fibrillare diventano substrato per l’enzima rame-dipendente lisil-ossidasi che deamina ossidativamente alcuni residui di lisina e idrossilisina, trasformando il gruppo amminico della loro catena laterale (-CH2-NH2) in un gruppo aldeidico (-CHO), convertendo così la lisina in allisina e l’idrossilisina in idrossiallisina. Questi gruppi aldeidici reattivi reagiscono per condensazione con i residui di lisina o idrossilisina delle molecole adiacenti a formare legami covalenti incrociati intermedi che possono evolvere, durante la maturazione del collagene, in addotti istidinici o, per aggiunta a un terzo residuo amminoacidico, in composti pirrolici o contenenti il gruppo piridinio. Questi legami sono responsabili della resistenza alla trazione delle fibre di collagene [Carlson, Exposito, Michelacci, Robins].
Nei tipi di collagene IV, VI, VII e XII (non fibrillari) i domini a tripla elica sono interrotti da segmenti non elicoidali. [Exposito, Sutmuller]
Digestione del collagene
Il collagene nativo è pressoché resistente agli enzimi proteolitici isolati, in parte anche a causa della sua insolubilità, ed è quindi considerato indigeribile. Tuttavia, il collagene denaturato può essere attaccato da numerosi enzimi proteolitici. La cottura e le condizioni di elevata acidità dell’ambiente gastrico (pH < 2,0) causano la denaturazione e lo svolgimento della tripla elica del collagene, rendendolo suscettibile alla digestione enzimatica. Pertanto, la gelatina e gli idrolizzati di gelatina preparati mediante idrolisi parziale della gelatina possono essere facilmente digeriti e assorbiti dall’intestino tenue [Asghar, Cerda, Taga].
Studi nutrizionali condotti su ratti hanno indicato che la digeribilità apparente7 del collagene da pelle bovina trattata con calce8 era del 90% ([Asghar, Whitmore]) e studi su volontari umani hanno dimostrato che, sebbene non tutta la proteina venga assorbita, il collagene9 viene digerito nella stessa misura di altre proteine [Reuterswärd].
Dopo l’ingestione, le proteine vengono scomposte in molecole più piccole prima di essere assorbite dal tratto gastrointestinale. Oltre ai singoli amminoacidi liberi, in condizioni normali anche alcuni peptidi e persino alcune macromolecole vengono assorbiti intatti nel tratto gastrointestinale e trasportati nel flusso sanguigno [Ichikawa, Iwai, Oesser, Ohara, Prockop, Shigemura, Shigemura3, Taga].
Diversi studi sono stati condotti su tessuti intestinali animali o su modelli di trasporto intestinale (solitamente basati su cellule Caco-210) per comprendere come vengono assorbiti i diversi peptidi ([Aito-Inoue, Matsui]). È noto che i di- e i tripeptidi possono essere trasportati attraverso il trasportatore di peptidi della membrana dell’orletto a spazzola PepT1, mentre le vie di trasporto intestinale degli oligopeptidi con 4 o più residui amminoacidici rimangono sconosciute. Secondo quanto è stato finora riportato, questi ultimi oligopeptidi sono principalmente coinvolti in vie di diffusione passiva attraverso tight junctions paracellulari [Matsui, Xu].
In alcuni esperimenti ex vivo sull’intestino tenue dei topi, sono stati riscontrati peptidi con un peso molecolare (PM) compreso tra 1 kD e ~10 kD sul lato sieroso dell’intestino dopo l’applicazione di un idrolizzato di gelatina, indicando che possono essere assorbite quantità significativa di proteine del lisato ad alto PM [Oesser].
I peptidi e le proteine macromolecolari assorbiti intatti dall’intestino mantengono alcune funzioni biologiche, suggerendo la possibilità per i peptidi le e proteine somministrati per via orale di possedere un effetto terapeutico [Oesser].
Il collagene (e quindi anche la gelatina) è l’unica proteina animale che contiene quantità significative di idrossiprolina11. Praticamente quasi tutta l’idrossiprolina presente nei tessuti e nei fluidi animali è presente come componente del collagene oppure sotto forma di peptidi o idrossiprolina libera derivata dalla degradazione del collagene [Cerda].
Dopo l’ingestione di gelatina da parte di soggetti adulti normali, fino all’8% dell’idrossiprolina presente nella gelatina viene assorbita e poi escreta nelle urine in forma legata, come componente di peptidi [Cerda, Prockop].
Oltre 50 anni fa, Prockop et al. hanno segnalato per la prima volta che peptidi contenenti Hyp compaiono nel sangue a concentrazioni relativamente elevate dopo l’ingestione orale di idrolizzato di gelatina, sebbene la struttura del peptide non fosse stata determinata [Prockop, Taga].
Più di recente, alcuni ricercatori hanno identificato un gruppo di di- e tripeptidi contenenti idrossiprolina (Hyp) nel sangue di volontari dopo l’ingestione orale di idrolizzato di gelatina e hanno rivelato che il peptide prolina-idrossiprolina (Pro-Hyp) rappresenta sempre una quota importante dei peptidi contenenti idrossiprolina derivati dal collagene, indipendentemente dalla provenienza animale della gelatina. Altri peptidi contenenti idrossiprolina sono stati identificati nel sangue, tra cui Ala-Hyp, Ile-Hyp, Leu-Hyp, Phe-Hyp, Hyp-Gly, Ala-Hyp-Gly, Pro-Hyp-Gly e Ser-Hyp-Gly. Gli oligopeptidi derivati dal collagene sono stati rilevati nel sangue a concentrazioni significativamente più elevate dopo l’ingestione, probabilmente a causa della loro maggiore resistenza alle proteasi del sangue [Iwai, Ohara, Shigemura, Taga].
Alcuni studi hanno evidenziato che non tutto il collagene è equivalente. Ad esempio, il collagene della pelle del pesce Salmo salar e il collagene del tendine d’Achille bovino non contengono affatto cisteina, mentre piccole quantità di questo amminoacido sono presenti nel collagene del femore bovino. Il tendine d’Achille bovino contiene circa il 30% di idrossiprolina in più rispetto alla pelle del pesce e il collagene del femore ne contiene ancora di più (circa il doppio rispetto alla pelle del pesce) [Gauza-Włodarczyk].
Inoltre, alcuni peptidi contenenti idrossiprolina compaiono nel sangue solo dopo l’ingestione di gelatina prodotta da specifici animali. Nella tabella 2 sono riportati alcuni esempi [Ichikawa, Iwai, Ohara].
|
Sequenza |
cotenna di maiale |
squame di pescec |
pelle di pescec |
zampe di pollo |
cartilagine di pollo |
|
Ala-Hyp |
nda |
15% |
15% |
N/Ab |
N/A |
|
Ala-Hyp-Gly |
nd |
16% |
nd |
>3% |
>4% |
|
Ser-Hyp-Gly |
nd |
12% |
nd |
N/A |
N/A |
|
Pro-Hyp |
95% |
39% |
42% |
92% |
>70% |
|
Pro-Hyp-Gly |
nd |
5% |
3% |
>3% |
>19% |
|
Ile-Hyp |
>1% |
2% |
7% |
>1% |
>1% |
|
Leu-Hyp |
>3% |
10% |
27% |
>1% |
>5% |
|
Phe-Hyp |
>1% |
3% |
7% |
>1% |
>1% |
Tabella 2: Peptidi di collagene recuperati in modo semiquantitativo nel plasma umano dopo l’ingestione orale di idrolizzati di gelatina (anon rilevato, bdati non disponibili, cspecie di pesce non note). Adattato da [Ichikawa, Iwai, Ohara].
In un singolo studio su ratti, l’autoradiografia dell’intero corpo a 30 minuti dalla somministrazione orale di [14C]-Pro-Hyp ha mostrato un’ampia distribuzione della radioattività nell’organismo, comprendendo anche la pelle e le cartilagini articolari. Il livello più elevato di radioattività è stato osservato nelle pareti gastriche e intestinali. È stata altresì notata l’incorporazione della radioattività in cellule note per rispondere all’oligopeptide Pro-Hyp, come i fibroblasti dermici, le cellule sinoviali, i condrociti, gli osteoblasti e gli osteoclasti [Kawaguchi].
L’analisi dei metaboliti di [14C]-Pro-Hyp nei tessuti e nel plasma ha mostrato che Pro-Hyp è parzialmente distribuito nei tessuti osservati in forma intatta e questo potrebbe dar ragione delle funzioni biologiche del dipeptide [Kawaguchi].
Negli animali, la maggior parte (quasi il 90%) della trans-4-idrossi-L-prolina derivata dal collagene viene catabolizzata a Gly attraverso la via della trans-4-idrossi-L-prolina ossidasi, mentre la trans-3-idrossi-L-prolina viene degradata attraverso la via della trans-3-idrossi-L-prolina deidratasi in ornitina e glutammato, conservando così la prolina e l’arginina di origine alimentare ed endogene [Hu].
Cinetica
Shigemura et al. hanno verificato le variazioni nel tempo delle concentrazioni di Hyp libera e incorporata in peptidi nel plasma di volontari umani a seguito dell’ingestione di un idrolizzato di collagene preparato da gelatina di pelle di merluzzo (Gadus macrocephalus) mediante idrolisi enzimatica [Shigemura3].
Le concentrazioni di entrambe le forme di Hyp hanno iniziato ad aumentare a 0,5 ore e hanno raggiunto il livello massimo entro 2 ore dall’ingestione dell’idrolizzato. La concentrazione plasmatica dei peptidi contenenti Hyp è aumentata in modo dose-dipendente, raggiungendo livelli massimi di 6,43, 20,17 e 32,84 nmol/ml dopo l’ingestione di dosi rispettivamente di 30,8, 153,8 e 384,6 mg/kg di collagene idrolizzato. Sebbene il livello di Hyp libera sia diminuito a due terzi del suo massimo 6 ore dopo l’ingestione, tale livello è rimasto comunque significativamente più alto rispetto a prima dell’ingestione. Dopo 4-6 ore dall’ingestione, il livello di peptidi contenenti Hyp è tornato al livello pre-ingestione. Un quarto della quantità massima di Hyp totale (libera + incorpora nei peptidi) nel plasma era presente sotto forma di peptidi contenenti Hyp [Shigemura3].
I risultati hanno mostrato che l’ingestione di oltre 153,8 mg (per kg di peso corporeo) di idrolizzato di collagene ha aumentato significativamente i livelli plasmatici di Hyp libera e incorporata in peptidi. Tuttavia, l’ingestione di una dose di 30,8 mg di idrolizzato di collagene non ha avuto un effetto significativo sul livello plasmatico di entrambe le forme di Hyp [Shigemura3].
Secondo gli autori, i risultati suggeriscono che l’ingestione di una dose di soli 30,8 mg di idrolizzato di collagene potrebbe non essere efficace nel promuovere effetti benefici su pelle, articolazioni e concentrazioni di lipidi nel sangue. Non è stato osservato alcun limite nella quantità di Hyp che può essere assorbita nel plasma con l’ingestione fino a 384,6 mg di idrolizzato di collagene per kg di peso corporeo. Pertanto, l’ingestione di dosi maggiori di idrolizzato di collagene può migliorare la distribuzione dei peptidi contenenti Hyp di origine alimentare nei tessuti e i conseguenti effetti benefici su pelle e articolazioni [Shigemura3].
Collagene e gelatina nella medicina tradizionale e popolare
La gelatina è utilizzata nella medicina popolare e tradizionale dell’Asia da tempi immemorabili. Nella medicina cinese, una speciale gelatina a base di pelle d’asino (阿膠, E Jiao, Colla Corii Asini) viene utilizzata per tonificare e nutrire il sangue, fermare le emorragie, nutrire e umidificare lo Yin e idratare i polmoni e l’intestino crasso [AmDragon, Kubo, Shigemura4].
Secondo lo Shennong Bencao Jing (Materia Medica Classica di Shennong), testo compilato tra il I e il II secolo d.C., l’E Jiao è utile anche per prevenire l’aborto spontaneo e stabilizzare le condizioni dei nascituri e delle donne incinte [Kubo].
Probabilmente l’E Jiao non veniva ricavato dalla pelle d’asino, come avviene oggi, prima della dinastia Tang (618-907 d.C.). Al suo posto, si utilizzava la pelle di altri animali, principalmente quella bovina. La materia prima principale per l’E Jiao passò dalla pelle di mucca a quella d’asino tra la dinastia Tang e la dinastia Song (960-1276 d.C.). Oggi, la gelatina di pelle di bue viene utilizzata per produrre la Huang Ming Jiao (黄明胶, Colla Corii Bovis), utilizzata per tonificare lo Yin e umidificare la secchezza, per arrestare le emorragie e per risolvere le tumefazioni [Kubo, TCMWiki].
La gelatina di pesce viene utilizzata per produrre la Yu Biao (鱼鳔, oppure 鱼膠, Yu Jiao, Colla Pisces), utilizzata per nutrire lo Yin, sottomettere lo Yang e nutrire Fegato e Reni (in caso di emissione di seme, calo della libido, debolezza e indolenzimento della parte bassa della schiena e delle ginocchia, tosse), per arrestare le emorragie, dissipare la Stasi di Sangue e risolvere le tumefazioni, e per calmare il feto. Viene utilizzato anche in caso di tetano e convulsioni postpartum [AmDragon].
Altri tipi di gelatina sono utilizzati nella medicina cinese, ad esempio la gelatina di guscio di tartaruga (龟板胶, Gui Ban Jiao, Colla Plastrum Testudinis). Recentemente, la gelatina di pelle di maiale (新阿胶, Xin E Jiao, “nuovo” E Jiao) è stata ritenuta un valido sostituto dell’E Jiao [Zhao].
L’uso medicinale della gelatina animale è quasi esclusivo di Cina, Giappone e altri paesi dell’Asia orientale. In Europa, Ildegarda di Bingen, nel suo libro “Physica” (datato intorno al 1150 d.C.), raccomandava pasti frequenti e abbondanti di brodo prodotto con frammenti di vitello, molto ricchi di collagene, per alleviare i dolori articolari [Kubo, Shigemura4, Silvestrini].
Usi moderni del collagene e dei suoi derivati
L’uso della gelatina per facilitare la deglutizione dei farmaci fu introdotto da un farmacista francese, François Mothes, nel XIX secolo. Nel 1896, A. Dastre e N. Floresco somministrarono ai cani un’iniezione endovenosa di soluzione di gelatina come trattamento per favorire la coagulazione del sangue senza trombosi. Questo è il primo uso medicinale della gelatina nell’Occidente moderno. [Kubo]
Alcuni studi in vivo su esseri umani e animali hanno dimostrato che l’ingestione di gelatina ha interessanti effetti sulla salute; ad esempio, migliora le condizioni delle unghie fragili e aumenta il diametro dei peli [Rosenberg, Scala, Shigemura4], migliora l’assorbimento del ferro non eme (regolando l’omeostasi sistemica del ferro piuttosto che solubilizzando il ferro ferrico luminale) [Wu], protegge dalla colite indotta sperimentalmente [Zhu].
Recentemente, i peptidi di collagene (cioè il collagene idrolizzato) sono stati proposti per il trattamento di diversi problemi di salute, nonché per scopi estetici. Tramite l’idrolisi, le lunghe catene insolubili di amminoacidi del collagene vengono scomposte in peptidi più piccoli, solubili in acqua e considerati più digeribili e meglio assorbibili sia rispetto al collagene che alla gelatina.
La prima applicazione terapeutica del collagene idrolizzato risale alla seconda metà del XX secolo, quando negli Stati Uniti venne utilizzato principalmente per trattare le affezioni degli annessi cutanei, più tipicamente la debolezza delle unghie, delle quali migliorava la crescita e la resistenza [Silvestrini].
La capacità del collagene idrolizzato di migliorare l’elasticità di tendini e legamenti, ridurre il dolore articolare e aumentare il tono della pelle è ormai ampiamente riconosciuta (e pubblicizzata).
Alcuni degli effetti benefici dell’ingestione di gelatina e collagene idrolizzato sono attribuiti alla Gly (un amminoacido condizionatamente essenziale con attività antinfiammatoria, immunomodulatrice e citoprotettiva), alla Hyp e agli oligopeptidi contenenti Hyp, in particolare Pro-Hyp, che costituiscono i principali prodotti che si ritrovano nel circolo sanguigno dopo l’ingestione e la digestione della gelatina alimentare [Cerda, Wu].
Collagene idrolizzato: studi in vitro
Recenti studi in vitro hanno dimostrato che i peptidi contenenti idrossiprolina hanno diverse interessanti funzioni fisiologiche [Minaguchi, Nakatani, Ohara2, Shigemura, Shigemura2, Taga, Wu]. Si è scoperto, ad esempio, che sono in grado di:
- stimolare la crescita dei fibroblasti cutanei e la produzione di collagene (principalmente Pro-Hyp e Hyp-Gly) [Nakatani, Ohara2, Shigemura, Shigemura2, Shigemura3, Taga], un processo notoriamente regolato dalla presenza di acido ascorbico [Murad, Taga];
- promuovere la differenziazione di osteoblasti, mioblasti, condrociti, preadipociti e cellule T helper [Wu];
- aumentare la sintesi di acido ialuronico nei fibroblasti, nei condrociti e nelle cellule sinoviali [Wu];
- inibire la mineralizzazione dei condrociti [Nakatani, Shigemura3].
Questi dati suggeriscono che i peptidi del collagene contenenti idrossiprolina potrebbero essere associati al processo di guarigione delle ferite e delle infiammazioni [Iwai].
Pro-Hyp-Gly, Pro-Hyp e alcuni altri peptidi contenenti idrossiprolina hanno attività chemiotattica sui fibroblasti e su neutrofili e monociti del sangue periferico [Ichikawa, Iwai, Laskin, Postlethwaite, Postlethwaite2]. Ala-Hyp e Gly-Pro-Val sono potenziali inibitori dell’enzima di conversione dell’angiotensina [Kim, Iwai, Oshima].
Sfortunatamente, solo pochi studi hanno confrontato gli effetti dei peptidi contenenti Hyp con una miscela degli aminoacidi costituenti come controllo. In un paio di studi, gli effetti di Pro-Hyp sono stati confrontati con Pro e Hyp da soli e/o con una miscela di Pro e Hyp e né gli aminoacidi da soli né la loro miscela sono stati in grado di produrre gli stessi effetti del dipeptide Pro-Hyp. [Minaguchi, Nakatani]
In ogni caso, l’integrazione di Pro da sola si è dimostrata incapace di aumentare la produzione di collagene nei CAF (Carcinoma-Associated Fibroblasts) mammari umani e nei fibroblasti cutanei umani, a meno che la disponibilità di glutammina (Gln) o la sintesi di Pro12 non fossero limitate. Inoltre, sebbene la Pro esogena aumenti l’espressione di COL1A113 e la Pro radiomarcata venga incorporata nel collagene nei fibroblasti dermici umani, questo effetto è più pronunciato quando i fibroblasti vengono coltivati in assenza di Gln. Pertanto, sembra che i fibroblasti sintetizzino preferenzialmente la propria Pro. Ciò suggerisce che la disponibilità di Pro determina il tasso di biosintesi del collagene, mentre la domanda di Pro nei fibroblasti è soddisfatta principalmente dalla conversione da Gln [Karna, Kay, Szoka].
In un singolo esperimento, la somministrazione orale di Hyp per due settimane in dosi di 0,5 o 1 g/kg a ratti maschi ha aumentato il contenuto di collagene solubile nella pelle, suggerendo che la somministrazione orale di Hyp abbia incrementato la produzione di collagene [Aoki].
Collagene idrolizzato: studi in vivo
Alcuni studi hanno esaminato gli effetti dell’ingestione di collagene idrolizzato da parte di animali o volontari umani.
In uno studio preclinico, sono stati studiati gli effetti dell’assunzione giornaliera di 7 g di una miscela di idrolizzato di collagene commerciale contenente 5 g di idrolizzato di collagene di tipo I sulle caratteristiche della pelle di 25 volontarie giapponesi che tendevano ad avere la pelle secca e ruvida in inverno. Dopo 6 settimane di ingestione, il contenuto di umidità dello strato corneo di viso, guance, avambraccio e nuca è aumentato, suggerendo un miglioramento delle condizioni della pelle. Anche le proprietà viscoelastiche, tra cui flessibilità ed elasticità, sono migliorate significativamente. L’analisi microscopica ha inoltre mostrato un miglioramento significativo delle caratteristiche della superficie della pelle delle guance, come maggiore levigatezza, riduzione delle rughe e minore ruvidità. Inoltre, il pH superficiale della pelle è rimasto invariato a un pH debolmente acido di 5,9 durante l’intero periodo di studio, segno del mantenimento di buone condizioni cutanee [Matsumoto].
In uno studio con placebo, sono stati esaminati gli effetti dell’ingestione giornaliera di 2,5 o 5 g di idrolizzati di collagene suino di tipo I sui parametri cutanei relativi all’invecchiamento cutaneo in 69 donne di età compresa tra i 35 e i 55 anni. Dopo 8 settimane di ingestione, è stato osservato un aumento significativo dell’elasticità cutanea in entrambi i gruppi trattati con idrolizzato di collagene rispetto al gruppo placebo. A 4 settimane dall’ultima ingestione, nel gruppo di trattamento si è osservato un più duraturo effetto fisiologico positivo rispetto all’elasticità cutanea nelle donne di età superiore ai 50 anni. Inoltre, è stato osservato un effetto positivo dell’ingestione di idrolizzati di collagene anche rispetto all’idratazione e alla traspirazione cutanee nelle donne meno giovani [Proksch].
In un esperimento su topi, è stato esaminato l’effetto dell’ingestione giornaliera di peptidi di collagene (0,2 g/kg di peso corporeo) preparati a partire da squame di pesce sul danno cutaneo indotto da ripetute irradiazioni con raggi UV-B. L’ingestione dei peptidi di collagene ha contrastato la riduzione dell’idratazione cutanea, l’iperplasia dell’epidermide e la diminuzione del collagene solubile di tipo I indotta dai raggi UV-B [Tanaka].
Per studiare gli effetti dell’ingestione di peptidi di collagene sui fibroblasti e sulla matrice extracellulare del derma, sono stati somministrati peptidi di collagene per via orale a suini alla dose di 0,2 g/kg di peso corporeo/giorno per 62 giorni e gli effetti sono stati confrontati con quelli di un gruppo di controllo che assumeva lattoalbumina e acqua. La densità dei fibroblasti, il diametro e la densità delle fibrille di collagene erano significativamente maggiori nel gruppo trattato con peptidi di collagene rispetto ai gruppi trattati con lattoalbumina e acqua. I due principali componenti dei glicosaminoglicani dermici, acido ialuronico e dermatan solfato, presenti nello spazio interfibrillare, non differivano significativamente tra i tre gruppi. Tuttavia, la quantità di dermatan solfato, che deriva dalla decorina legata alle fibrille, era maggiore nel gruppo trattato con peptidi di collagene. Questi risultati suggeriscono che l’ingestione di peptidi di collagene induce una maggiore densità dei fibroblasti e migliora la formazione di fibrille di collagene nel derma [Matsuda].
Collagene idrolizzato per scopi estetici
Il collagene idrolizzato viene utilizzato come integratore mirato principalmente a contrastare i segni dell’invecchiamento.
Con l’età la produzione di collagene si riduce mentre aumenta la sua degradazione. Questa è causata da fattori interni (ormonali e metabolici) o esterni, come la continua esposizione ai raggi UV e l’inquinamento.
La diminuzione del collagene nel nostro corpo è tra le cause di:
- perdita di tonicità della pelle;
- tendenza alla riduzione della massa muscolare (sarcopenia);
- fragilità ossea (osteoporosi);
- dolori e degenerazione delle cartilagini (artrite) [Meritene].
L’assunzione di collagene idrolizzato viene suggerito come utile ad attenuare tutti questi processi tipici dell’invecchiamento e, in particolare, per:
- migliorare elasticità, tonicità e compattezza della pelle;
- ridurre i dolori articolari e ossei da artrite e osteoartrite;
- contribuire a mantenere e sviluppare massa muscolare supportando la lotta alla sarcopenia;
- rafforzare unghie e capelli [Meritene].
Come abbiamo già visto (vedi paragrafi precedenti), la ricerca sembra per lo più confermare le affermazioni di cui sopra. In ogni caso, va detto che la maggior parte degli studi finora condotti è stata condotta in vitro o in vivo su animali, oppure su piccole coorti di volontari umani per periodi di tempo relativamente brevi. Inoltre, le dosi, le fonti (bovina, suina, marina, ecc.) e i pesi molecolari dei peptidi utilizzati negli esperimenti variano notevolmente tra gli studi, rendendo le condizioni troppo eterogenee per ottenere risultati coerenti. Infine, ultimo ma non meno importante, molti studi sono stati sponsorizzati dall’industria, soprattutto quelli riguardanti i presunti effetti estetici.
Collagene marino e collagene da mammiferi
Il collagene utilizzato per la produzione dei derivati idrolizzati deriva in gran parte dagli scarti di macellazione (pelli, ossa, legamenti, cartilagini, …) di animali come bovini, suini e cavalli. Molti produttori, tuttavia, preferiscono utilizzare il cosiddetto collagene marino, ottenuto dagli scarti della lavorazione del pesce.
Talvolta si trovano in commercio prodotti preparati con collagene vegetale o collagene vegano, ma, in realtà, tali prodotti contengono solo sostanze o miscele di sostanze che imitano il collagene per consistenza (specialmente nei prodotti cosmetici per uso esterno) o composizione, in quanto il collagene non esiste nel regno vegetale.
Nei prodotti di origine ittica e in quelli ottenuti da pelli animali, il tipo di collagene di partenza è prevalentemente di tipo I; nei derivati ottenuti a partire da ossa, legamenti, cartilagini si trovano anche quantità variabili di collagene di tipo II e III.
Il collagene di tipo I è quello più comunemente utilizzato per la cura della salute e della bellezza della pelle, mentre il collagene di tipo II è quello preferito e maggiormente utilizzato per il trattamento delle articolazioni [Campos].
Inoltre, i produttori spesso arrivano a dire esplicitamente al consumatore che un determinato tipo di collagene è più adatto di un altro per uno scopo specifico, ad esempio il collagene di tipo I idrolizzato o il collagene di pesce idrolizzato “fanno più bene” alla pelle perché la pelle è composta principalmente da collagene di tipo I (vedi ad esempio il box 1), ma la ragione alla base di questa affermazione è piuttosto debole: non c’è motivo per cui un determinato tipo di derivato del collagene, una volta digerito dagli enzimi gastrointestinali e infine dalle proteasi del sangue (vedi, ad esempio, [Matsui]), venga riciclato dall’organismo per ricostituire lo stesso tipo di collagene (o addirittura il collagene in genere).
|
Nel collagene marino idrolizzato troviamo soprattutto collagene Tipo I. Al contrario, nel collagene bovino idrolizzato troviamo il Tipo II e Tipo III. Per questo di solito si usa il collagene marino per migliorare la pelle, rallentare l’invecchiamento e supportare la mobilità di tendini e legamenti. Mentre il collagene idrolizzato bovino può essere consigliato per problemi alle cartilagini, artrite o rinforzo muscolare. |
Box 1: Un claim sulla differenza tra il collagene idrolizzato di pesce e quello bovino [Meritene]
Sono stati condotti diversi studi in vitro o ex vivo per studiare l’assorbibilità gastrointestinale dei peptidi (vedi paragrafo “Digestione del collagene“), ma le uniche molecole che vengono assorbite dall’organismo umano (e che quindi possono esercitare funzioni biologiche) con certezza sono quelle ritrovate in vivo nei campioni di sangue dopo l’ingestione di collagene (idrolizzato) (vedi anche [Matsui]).
Gli amminoacidi liberi e i peptidi presenti nel sangue dopo l’assunzione di derivati del collagene variano significativamente al variare sia del tipo di animale da cui è estratto il collagene sia delle parti dell’animale utilizzato, anche nel caso in cui il tipo di collagene sia lo stesso (vedi, ad esempio, tabella 2). I principali peptidi per i quali è stata riconosciuta un’attività di stimolazione dei fibroblasti in vitro sono Pro-Hyp e Hyp-Gly, ossia i principali peptidi presenti nel sangue dopo l’assunzione di collagene estratto da qualsivoglia materia prima14, il che significa che tutto il collagene può avere un impatto positivo sulla salute della pelle, quale che sia la sua provenienza.
Inoltre, il collagene marino, che è per lo più di tipo I, ha dimostrato, ex vivo, in vitro o in vivo su volontari umani o animali, di avere la capacità di facilitare la guarigione delle ferite (vedi, ad esempio, [de Souza]), di modulare il metabolismo della cartilagine [Boonmaleerat] e di avere un impatto positivo sulla rigenerazione ossea [Yamada], attività che nel corpo umano coinvolgono anche il collagene di tipo II e di tipo III.
Anche le affermazioni su una migliore o più rapida assimilabilità del collagene di pesce (vedi ad esempio il box 2) non hanno alcun valore reale, almeno quando si tratta di prodotti idrolizzati (la velocità di assorbimento, in questo caso, dipende da diversi fattori, tra cui il peso molecolare medio dei peptidi ottenuti per idrolisi).
Il collagene marino presenta alcuni reali vantaggi rispetto al collagene di mammiferi.
In primo luogo, il collagene marino può essere consumato anche da persone che, per motivi culturali o religiosi, non possono mangiare carne in generale o determinati tipi di carne (es., suina o bovina). In secondo luogo, il collagene marino non è possibile fonte di trasmissione di malattie che possono destare preoccupazione per la salute umana (come le encefalopatie spongiformi o l’influenza aviaria).
|
Il collagene di pesce viene assorbito dall’organismo fino a 1,5 volte più efficacemente, il che significa che ha una biodisponibilità superiore rispetto a quello bovino o suino. Poiché viene assorbito in modo più efficiente e raggiunge il flusso sanguigno più rapidamente, è considerato la migliore fonte di collagene per applicazioni farmaceutiche. |
Box 2: Un claim sull’assorbibilità del collagene di pesce [Sripriya]
Inoltre, gli scarti della macellazione animale sono spesso utilizzati come materie prime dall’industria conciaria e dall’industria alimentare (es., per la preparazione di carni in gelatina o gelatine pronte all’uso per le preparazioni alimentari), mentre gli scarti della lavorazione del pesce sono normalmente considerati un sottoprodotto di scarsa o nulla importanza industriale. Ad oggi, gli scarti di pesce sono in parte destinati alla produzione di farina di pesce, fertilizzanti e olio di pesce, tutti prodotti con scarsa redditività, e in parte utilizzati come materia prima per l’alimentazione dei pesci in acquacoltura, ma un’enorme quantità di tali scarti viene gettata via [Coppola, Guillen]. Ciò può avere un impatto sul prezzo e sulla disponibilità delle materie prime.
D’altra parte, la maggior parte del collagene di pesce contiene meno Pro e Hyp rispetto al collagene di origine mammifera [Oslan].
In più, il collagene marino può avere un odore residuo di pesce se non viene lavorato correttamente [WangX].
Tossicità del collagene
Il collagene idrolizzato è un materiale sicuro sia per uso interno che esterno (ad esempio, cosmetico), con una debole antigenicità. È risultato praticamente atossico quando somministrato per via orale o dermica in studi di tossicità acuta sugli animali. Questo ingrediente è risultato minimamente irritante per gli occhi dei conigli e anche i test di irritazione cutanea nei conigli hanno indicato che il collagene idrolizzato è risultato non irritante o minimamente irritante. Studi dermici di tossicità subcronica su due formulazioni cosmetiche contenenti il 2% di collagene idrolizzato sono risultati negativi per tossicità sistemica. Il collagene idrolizzato non ha avuto effetti sensibilizzanti nelle cavie. Negli studi clinici, il collagene idrolizzato non ha prodotto irritazione cutanea, sensibilizzazione o indicazione di fototossicità [Aguirre-Cruz, CIR].
Bibliografia
|
[Aguirre-Cruz] |
Aguirre-Cruz, G. et al.,“Collagen Hydrolysates for Skin Protection: Oral Administration and Topical Formulation”, Antioxidants (Basel). 2020 Feb 22;9(2):181. doi: 10.3390/antiox9020181. |
|
[Aito-Inoue] |
Aito-Inoue, M. et al., “Transport of a tripeptide, Gly-Pro-Hyp, across the porcine intestinal brush-border membrane”, J Pept Sci. 2007 Jul;13(7):468-74. doi: 10.1002/psc.870. |
|
[AmDragon] |
American Dragon, https://www.americandragon.com/ |
|
[Aoki] |
Aoki, M. et al., “Increasing effect of an oral intake of L-hydroxyproline on the soluble collagen content of skin and collagen fragments in rat serum”; Biosci Biotechnol Biochem. 2012;76(6):1242-4. doi: 10.1271/bbb.120058. |
|
[Asghar] |
Asghar, A., Henrickson, R. L., “Chemical, biochemical, functional, and nutritional characteristics of collagen in food systems”, Adv Food Res. 1982:28:231-372. doi: 10.1016/s0065-2628(08)60113-5. |
|
[Boonmaleerat] |
Boonmaleerat, K. et al., “Fish Collagen Hydrolysates Modulate Cartilage Metabolism”, Cell Biochem Biophys. 2018 Jun;76(1-2):279-292. doi: 10.1007/s12013-017-0817-2. |
|
[Campos] |
Patrícia Maria Berardo Gonçalves Maia Campos et al.,“Oral Supplementation with Hydrolyzed Fish Cartilage Improves the Morphological and Structural Characteristics of the Skin: A Double-Blind, Placebo-Controlled Clinical Study”, Randomized Controlled Trial Molecules. 2021 Aug 12;26(16):4880. doi: 10.3390/molecules26164880. |
|
[Canty] |
Canty E. G. et al., “Procollagen trafficking, processing and fibrillogenesis”, J Cell Sci. 2005 Apr 1;118(Pt 7):1341-53. doi: 10.1242/jcs.01731. doi: 10.1242/jcs.01731. |
|
[Carlson] |
Carlson, B. M., “Chapter 2 – Tissues”. doi: 10.1016/B978-0-12-804254-0.00002-8. In: “The Human Body – Linking Structure and Function” (2018), ISBN: 978-0-12-804254-0, doi: 10.1016/C2015-0-00205-2. |
|
[Cerda] |
Cerda J. J. et al., “Intraduodenal hydrolysis of gelatin as a measure of protein digestion in normal subjects and in patients with malabsorption syndromes”, Gastroenterology. 1968 Mar;54(3):358-65. doi: 10.1016/S0016-5085(68)80096-4]. |
|
[CIR] |
CIR, “7 Final Report on the Safety Assessment of Hydrolyzed Collagen”, Cosmetic Ingredient Review. J. Am. Coll. Toxicol. 1985;4:199–221. doi: 10.3109/10915818509078691. |
|
[Coppola] |
Coppola, D. et al.,“Fish Waste: From Problem to Valuable Resource”, Mar Drugs. 2021 Feb 19;19(2):116. doi: 10.3390/md19020116. |
|
[de Souza] |
de Souza A. et al., “Fish collagen for skin wound healing: a systematic review in experimental animal studies”, Cell Tissue Res. 2022 Jun;388(3):489-502. doi: 10.1007/s00441-022-03625-w. |
|
[Exposito] |
Jean-Yves Exposito et al, “The Fibrillar Collagen Family”, Int. J. Mol. Sci. 2010, 11, 407-426. doi: 10.3390/ijms11020407. |
|
[Gauza-Włodarczyk] |
Gauza-Włodarczyk, M. et al., “Amino acid composition in determination of collagen origin and assessment of physical factors effects”, Int J Biol Macromol. 2017 Nov;104(Pt A):987-991. doi: 10.1016/j.ijbiomac.2017.07.013. |
|
[Gelse] |
Gelse, K. et al., “Collagens–structure, function, and biosynthesis”, Adv Drug Deliv Rev. 2003 Nov 28;55(12):1531-46. doi: 10.1016/j.addr.2003.08.002. |
|
[Guillen] |
Guillen, J. et al.,“A Review of the European Union Landing Obligation Focusing on Its Implications for Fisheries and the Environment”, Sustainability 2018, 10(4), 900. doi: 10.3390/su10040900. |
|
[Harwood] |
Harwood, R. et al., “Studies on the glycosylation of hydroxylysine residues during collagen biosynthesis and the subcellular localization of collagen galactosyltransferase and collagen glucosyltransferase in tendon and cartilage cells”, Biochem J. 1975 Nov;152(2):291-302. doi: 10.1042/bj1520291. doi: 10.1042/bj1520291. |
|
[Hu] |
Hu, S. et al., “Hydroxyproline in animal metabolism, nutrition, and cell signaling”, Amino Acids. 2022 Apr;54(4):513-528. doi: 10.1007/s00726-021-03056-x |
|
[Hulmes] |
Hulmes D.J.S. “Collagen diversity, synthesis and assembly”, In: “Collagen – Structure and Mechanics”. Mech. Fratzl P., editor. Springer Science+Business Media; 2008.; pp. 15–47. doi: 10.1007/978-0-387-73906-9_2. |
|
[Karna] |
Karna, E. et al., “Proline-dependent regulation of collagen metabolism”, Cell. Mol. Life Sci. 77, 1911–1918 (2020). doi: 10.1007/s00018-019-03363-3 |
|
[Kawaguchi] |
Kawaguchi T. et al, “Distribution of Prolylhydroxyproline and Its Metabolites after Oral Administration in Rats”, Biological and Pharmaceutical Bulletin, 2012, 35 (3), Pages 422-427. doi: 10.1248/bpb.35.422. |
|
[Kay] |
Kay EJ et al., “Regulation of Extracellular Matrix Production in Activated Fibroblasts: Roles of Amino Acid Metabolism in Collagen Synthesis”. Front. Oncol., 2021, 11:719922. doi: 10.3389/fonc.2021.719922 |
|
[Kim] |
Kim, S. K. et al.,“Angiotensin I converting enzyme inhibitory peptides purified from bovine skin gelatin hydrolysate”, J Agric Food Chem. 2001 Jun;49(6):2992-7. doi: 10.1021/jf001119u. |
|
[Kubo] |
Kubo, T. et al., “History of the Chinese Medicinal Gelatin”, Chinese Medicine and Culture (2022) 5:1. doi: 10.1097/MC9.0000000000000005. |
|
[Ichikawa] |
Ichikawa, S. et al., “Hydroxyproline-containing dipeptides and tripeptides quantified at high concentration in human blood after oral administration of gelatin hydrolysate”, Int J Food Sci Nutr. 2010 Feb;61(1):52-60. Doi: 10.3109/09637480903257711. |
|
[Iwai] |
Iwai, K. et al., “Identification of food-derived collagen peptides in human blood after oral ingestion of gelatin hydrolysates”. J. Agric. Food Chem. 2005, 53, 6531−6536. doi: 10.1021/jf050206p. |
|
[Laskin] |
Laskin, D. L. et al., “Chemotactic activity of collagen-like polypeptides for human peripheral blood neutrophils”, J Leukoc Biol. 1986 Mar;39(3):255-66. doi: 10.1002/jlb.39.3.255. |
|
[Matsuda] |
Matsuda, N. et al., “Effects of ingestion of collagen peptide on collagen fibrils and glycosaminoglycans in the dermis”, J Nutr Sci Vitaminol (Tokyo). 2006 Jun;52(3):211-5. doi: 10.3177/jnsv.52.211. |
|
[Matsui] |
Matsui, T., “Are Peptides Absorbable Compounds?”, J Agric Food Chem. 2018 Jan 17;66(2):393-394. doi: 10.1021/acs.jafc.7b05589. |
|
[Matsumoto] |
Matsumoto, H. et al., “Clinical effect of fish type I collagen hydrolysate on skin properties”. ITE Lett. 2006, 7:386–90 |
|
[Meritene] |
[https://www.meritene.it/salute/collagene-idrolizzato-a-cosa-serve] (Retrieved: 2025-04-15) |
|
[Michelacci] |
Michelacci, Y.M., “Collagens and proteoglycans of the corneal extracellular matrix”, Braz J Med Biol Res 36 (8), Aug 2003. doi: 10.1590/S0100-879X2003000800009. |
|
[Minaguchi] |
Minaguchi, J. Et al., “Effects of collagen-derived oligopeptide prolylhydroxyproline on differentiation of mouse 3T3-L1 preadipocytes”, Food Sci. Technol. Res. 2012, 18, 593−599. doi: 10.3136/fstr.18.593. |
|
[Murad] |
Murad, S. et al., “Regulation of collagen synthesis by ascorbic acid”, Proc. Natl. Acad. Sci. U.S.A. 1981, 78, 2879−2882. doi: 10.1073/pnas.78.5.2879. |
|
[Nakatani] |
Nakatani, S. et al., “Chondroprotective effect of the bioactive peptide prolyl-hydroxyproline in mouse articular cartilage in vitro and in vivo”, Osteoarthritis Cartilage 2009, 17, 1620−1627. doi: 10.1016/j.joca.2009.07.001. |
|
[Oesser] |
Oesser, S. et al., “Oral Administration of 14C Labeled Gelatin Hydrolysate Leads to an Accumulation of Radioactivity in Cartilage of Mice (C57/BL)”, J Nutr. 1999 Oct;129(10):1891-5. doi: 10.1093/jn/129.10.1891. |
|
[Ohara] |
Ohara H. et al., “Comparison of Quantity and Structures of Hydroxyproline-Containing Peptides in Human Blood after Oral Ingestion of Gelatin Hydrolysates from Different Sources”, J. Agric. Food Chem. 2007, 55, 1532-1535. doi: 10.1021/jf062834s. |
|
[Ohara2] |
Ohara, H. et al., “Collagen-derived dipeptide, prolinehydroxyproline, stimulates cell proliferation and hyaluronic acid synthesis in cultured human dermal fibroblasts”, J. Dermatol. 2010, 37, 330−338. doi: 10.1111/j.1346-8138.2010.00827.x. |
|
[Oshima] |
Oshima, G. et al, “Peptide inhibitors of angiotensin I-converting enzyme in digests of gelatin by bacterial collagenase”, Biochim Biophys Acta; 1979 Jan 12;566(1):128-37. doi: 10.1016/0005-2744(79)90255-9. doi: 10.1016/0005-2744(79)90255-9. |
|
[Oslan] |
Oslan, S. N. H. et al.,“Extraction and Characterization of Bioactive Fish By-Product Collagen as Promising for Potential Wound Healing Agent in Pharmaceutical Applications: Current Trend and Future Perspective”, Int J Food Sci. 2022 May 6:2022:9437878. doi: 10.1155/2022/9437878. |
|
[Postlethwaite] |
Postlethwaite, A. E. et al., “Chemotactic attraction of human fibroblasts to type I, II, and III collagens and collagen-derived peptides”, Proc. Natl. Acad. Sci. U.S.A. 1978,75, 871-875. doi: 10.1073/pnas.75.2.871. |
|
[Postlethwaite2] |
Postlethwaite, A. E. et al., “Collagen-and collagen peptide-induced chemotaxis of human blood monocytes”, J Exp Med. 1976 Jun 1;143(6):1299–1307. doi: 10.1084/jem.143.6.1299. |
|
[Prockop] |
Prockop, D. J. et al., “Gastrointestinal absorption and renal excretion of hydroxyproline peptides”. Lancet 1962, 2, 527−528: doi: 10.1016/S0140-6736(62)90400-2. |
|
[Proksch] |
Proksch E. et al.,“Oral supplementation of specific collagen peptides has beneficial effects on human skin physiology: a double-blind, placebo-controlled study”, Skin Pharmacol Physiol. 2014;27(1):47-55. doi: 10.1159/000351376. |
|
[Quan] |
Bryan D. Quan, Eli D. Sone, “Chapter Nine – Cryo-TEM Analysis of Collagen Fibrillar Structure”, Methods in Enzymology, Volume 532, 2013, Pages 189-205. doi: 10.1016/B978-0-12-416617-2.00009-6. |
|
[Reuterswärd] |
Laser Reuterswärd, A., Andersson, H., Asp N. G., “Digestibility of collagenous fermented sausage in man”, Meat Sci. 1985;14(2):105-21. doi: 10.1016/0309-1740(85)90086-5. |
|
[Robins] |
Robins, S. P., Brady, J. D., “Collagen Cross-Linking and Metabolism”. doi: 10.1016/B978-0-12-373884-4.00035-5. In: “Principles of Bone Biology”, 3.rd Edition, Volume I, 2008, Pages 319-334; ISBN: 978-0-12-373884-4. |
|
[Rosenberg] |
Rosenberg, S. et al., “Further Studies in the Use of Gelatin in the Treatment of Brittle Nails”, Arch Derm. 1957;76(3):330-335. doi: 10.1001/archderm.1957.01550210054006. |
|
[Scala] |
Scala J. et al., “Effect of daily gelatin ingestion on human scalp hair”, Nutr. Report Inter., 13, 579-592 (1976) |
|
[Shenoy] |
Shenoy, M et al. (May 09, 2022), “Collagen Structure, Synthesis, and Its Applications: A Systematic Review”. Cureus 14(5): e24856. doi:10.7759/cureus.24856. |
|
[Shigemura] |
Shigemura, Y. et al., “Identification of a novel food-derived collagen peptide, hydroxyprolyl-glycine, in human peripheral blood by pre-column derivatisation with phenyl isothiocyanate”, Food Chem. 2011, 129, 1019−1024. doi: 10.1016/j.foodchem.2011.05.066. |
|
[Shigemura2] |
Shigemura, Y. et al., “Effect of prolylhydroxyproline (Pro-Hyp), a food-derived collagen peptide in human blood, on growth of fibroblasts from mouse skin”, J. Agric. Food Chem. 2009, 57, 444−449. doi: 10.1021/jf802785h. |
|
[Shigemura3] |
Shigemura, Y. et al., “Changes in Composition and Content of Food-Derived Peptide in Human Blood after Daily Ingestion of Collagen Hydrolysate for 4 weeks”, J Sci Food Agric. 2018 Mar; 98(5):1944-1950. doi: 10.1002/jsfa.8677. |
|
[Shigemura4] |
Shigemura, Y. et al., “Dose-dependent changes in the levels of free and peptide forms of hydroxyproline in human plasma after collagen hydrolysate ingestion”, Food Chem., 159 (15), September 2014, Pages 328-332. doi: 10.1016/j.foodchem.2014.02.091. |
|
[Shoulders] |
Shoulders, M. D., “Collagen structure and stability”, Annu Rev Biochem. 2009:78:929-58. doi: 10.1146/annurev.biochem.77.032207.120833. |
|
[Silvestrini] |
Silvestrini, B. et al., “Collagen Involvement in Health, Disease, and Medicine”, IntechOpen (2022). doi: 10.5772/intechopen.101978. |
|
[Sripriya] |
Sripriya, R. et al., “A Novel Enzymatic Method for Preparation and Characterization of Collagen Film from Swim Bladder of Fish Rohu (Labeo rohita)”, Food and Nutrition Sciences, 2015, 06(15), Pages 1468-1478, Article ID:61421. doi: 10.4236/fns.2015.615151 |
|
[Sugihara] |
Sugihara, F. et al., “Quantification of hydroxyprolyl-glycine (Hyp-Gly) in human blood after ingestion of collagen hydrolysate”, J Biosci Bioeng. 2012 Feb;113(2):202-3. doi: 10.1016/j.jbiosc.2011.09.024. |
|
[Sutmuller] |
M. Sutmuller e al., “Collagen types Vlll and X, two non-fibrillar, short-chain collagens. Structure homologies, functions and involvement in pathology”, Histol Histopathol (1997) 12: 557-566. |
|
[Szoka] |
Szoka, L. et al.,“Exogenous proline stimulates type I collagen and HIF-1α expression and the process is attenuated by glutamine in human skin fibroblasts”, Mol Cell Biochem. 2017 Nov;435(1-2):197-206. doi: 10.1007/s11010-017-3069-y. |
|
[Taga] |
Taga, Y. et al., “Highly Accurate Quantification of Hydroxyproline-Containing Peptides in Blood Using a Protease Digest of Stable Isotope-Labeled Collagen”, J. Agric. Food Chem. 2014, 62, 12096−12102. doi: dx.doi.org/10.1021/jf5039597. |
|
[Tanaka] |
Tanaka, M. et al., “Effects of collagen peptide ingestion on UV-B-induced skin damage”, Biosci Biotechnol Biochem. 2009 Apr 23;73(4):930-2. doi: 10.1271/bbb.80649. |
|
[TCMWiki] |
https://tcmwiki.com/ |
|
[Wang] |
Wang, C., “Human lysyl hydroxylase isoforms: multifunctionality of human LH3 and the amino acids important for its collagen glycosyltransferase activities”, Academic Dissertation, Faculty of Science, University of Oulu, ISBN:9514267990; retrieved at https://urn.fi/URN:ISBN:9514267990] |
|
[WangX] |
Wang X. Et al., “Off-flavour compounds in collagen peptides from fish: Formation, detection and removal”, International Journal of Food Science and Technology 2023, 58, 1543–1563. doi: 10.1111/ijfs.15962. |
|
[Watford] |
Watford, M., “Glutamine metabolism and function in relation to proline synthesis and the safety of glutamine and proline supplementation”, J Nutr. 2008 Oct;138(10):2003S-2007S. doi: 10.1093/jn/138.10.2003S. |
|
[Whitmore] |
Whitmore, R. et al., “Digestibility and safety of limed hide collagen in rat feeding experiments”. J. Food Sci. 1975, 40, 101. doi: 10.1111/j.1365-2621.1975.tb03746.x. |
|
[Wikipedia] |
https://it.wikipedia.org and https://en.wikipedia.org |
|
[Wu] |
Wu, Lingyu et al., “Dietary gelatin enhances non-heme iron absorption possibly via regulation of systemic iron homeostasis in rats”, Journal of Functional Foods (2019) 59, 272-280. doi: 10.1016/j.jff.2019.06.005. |
|
[Xu] |
Xu, Q. et al., “Bioavailability of bioactive peptides derived from food proteins across the intestinal epithelial membrane: A review”, Trends in Food Sci Technol, 86, April 2019, Pages 399-411. doi: 10.1016/j.tifs.2019.02.050 |
|
[Yamada] |
Yamada, S. et al., “Functional roles of fish collagen peptides on bone regeneration”, Dent Mater J. 2021 Dec 1;40(6):1295-1302. doi: 10.4012/dmj.2020-446. |
|
[Zhao] |
Zhao, Zhongjie et al., “阿胶、新阿胶、黄明胶、马皮胶、杂皮胶的质量对比研究 —Ⅰ.氨基酸分析 [Comparative Study on the Quality of E Jiao, New E Jiao, Huang Ming Jiao, Horse Hide Gelatine, and Miscellaneous Hide Gelatine—I. Amino Acid Analysis]”, 天然产物研究与开发 (Natural Product Research and Development) 1991, 3: 49–59. doi:10.16333/j.1001-6880.1991.03.009. |
|
[Zhu] |
Zhu S, Huang M, Feng G, et al., “Gelatin versus its two major degradation products, prolylhydroxyproline and glycine, as supportive therapy in experimental colitis in mice”. Food Sci Nutr. 2018;6:1023–1031. https://doi.org/10.1002/fsn3.639. |
Note
1. Il triptofano è completamente assente; cistina e cisteina sono presenti in quantità molto piccole, circa 1 residuo aminoacidico ogni 1000.
2. Le porzioni telopeptidiche sono responsabili di alcune proprietà immunogeniche del collagene. Il trattamento con pepsina in ambiente acido permette di scindere le sequenze telopeptidiche dal tropocollagene ottenendo così l’atelocollagene. Questo processo preserva la struttura a tripla elica. L’atelocollagene è caratterizzato da una maggiore solubilità in acqua rispetto al tropocollagene e dall’assenza di proprietà immunogeniche. L’atelocollagene, spesso chiamato semplicemente “collagene”, è ampiamente utilizzato per preparare materiali industriali e per la ricerca biologica, in particolare per uso umano.
3. L’Hyp si ritrova come trans-4-idrossi-L-prolina (4Hyp), quando la prolina è idrossilata dalla prolil 4-idrossilasi (P4H), o, in misura molto minore, come trans-3-idrossi-L-prolina (3Hyp), quando la prolina è idrossilata dalla prolil 3-idrossilasi (P3H). Il loro rapporto è di circa 100:1. La 3Hyp è assente nei collageni di tipo III dei mammiferi (come quelli umani e bovini), presente nella misura di soli 1-2 residui di 3Hyp per catena nei collageni di tipo I e II, di 3-6 residui per catena nei collageni di tipo V e XI e di circa il 10% delle idrossiproline totali nei collageni di tipo IV delle membrane basali [Hu, Hulmes].
4. Nello scorbuto, la mancata idrossilazione delle proline e delle lisine causa la formazione di una tripla elica più lasca.
5. Studi recenti hanno mostrato che entrambe le attività glicosiltransferasiche sono esercitate dall’enzima multifunzionale LH3 (che risiede nel reticolo endoplasmatico) che, oltre ad essere una lisil-idrossilasi, è quindi anche una galattosiltransferasi (GT) e una glucosiltransferasi (GGT). LH3 è quindi in grado di catalizzare le tre reazioni consecutive necessarie per la formazione della glucosilgalattosil-idrossilisina [Hulmes, Wang].
6. Le catene α sono indicate con i simboli αi(T), dove T è un numero ordinale che indica il tipo di collagene (ad esempio, I per il collagene di tipo I) e i è un numero cardinale (1, 2, …, n) che indica il tipo di catena α all’interno del collagene di tipo T. Ad esempio, α1(I) è il primo tipo di catena α nel collagene di tipo 1, mentre α2(I) è il secondo tipo. Il collagene di tipo I contiene due catene α1(I) identiche e una singola catena α2(I) diversa, mentre il collagene di tipo III contiene solo catene α1(III), essendo un collagene omotrimerico.
7. La digeribilità apparente è una misura della quantità di proteine (%) disponibile per l’assorbimento e viene solitamente calcolata stimando l’azoto fecale e il corrispondente introito alimentare:
Digeribilità apparente = (azoto assunto con la dieta − azoto fecale) × 100 / azoto assunto con la dieta.
8. Un sottoprodotto della lavorazione della pelle. La calcinazione (ovvero il trattamento con calce, ossia idrossido di calcio) idrolizza parzialmente i legami covalenti del collagene fibroso.
9. Da cotenne di maiale raccolte da maiali di 6 mesi scottate in acqua a 60°C per 10 minuti secondo le procedure del macello [Reuterswärd].
10. Una linea cellulare immortalizzata di cellule di adenocarcinoma colorettale umano.
11. Oltre che nel collagene, l’idrossiprolina è presente in poche proteine. Le piante, non contenendo collagene, contengono molta meno idrossiprolina rispetto agli animali [Hu].
12. Nell’organismo la maggior parte della Pro viene sintetizzata a partire da L-glutammato che a sua volta viene prodotto a partire da Gln. All’interno degli enterociti, la Gln viene degradata a glutammato, che viene poi trasformato in glutammato-γ-semialdeide tramite la pirrolina 5-carbossilato (P5C) sintasi. La glutammato-γ-semialdeide produce spontaneamente P5C, che viene poi ridotta a prolina dalla P5C reduttasi. La Pro si forma nell’organismo anche a partire da arginina e ornitina che, attraverso l’azione della ornitina aminotransferasi, producono glutammato-γ-semialdeide e quindi Pro tramite la P5C reduttasi. L’espressione della P5C sintasi è tuttavia limitata all’intestino e pertanto questo organo è l’unico sito dell’organismo in cui la glutammina (glutammato) può comportarsi da precursore della sintesi della Pro. Nei ratti, circa il 7% del carbonio della glutammina metabolizzato nell’intestino tenue del ratto è utilizzato per la sintesi della prolina [Watford].
13. Il gene responsabile della sintesi della catena pro-α1 nel collagene di tipo I.
14. Mentre Pro-Hyp è il principale peptide presente nel sangue dopo l’assunzione di qualsiasi tipo di collagene, Hyp-Gly è stato trovato solo dopo l’ingestione di collagene idrolizzato ricavato da squame di pesce e pelle di maiale (vedere ad esempio [Shigemura, Shigemura3, Sugihara]).
Immagine in evidenza di Ernesto Rodriguez da Pixabay




